11/06/2021 - 18:35
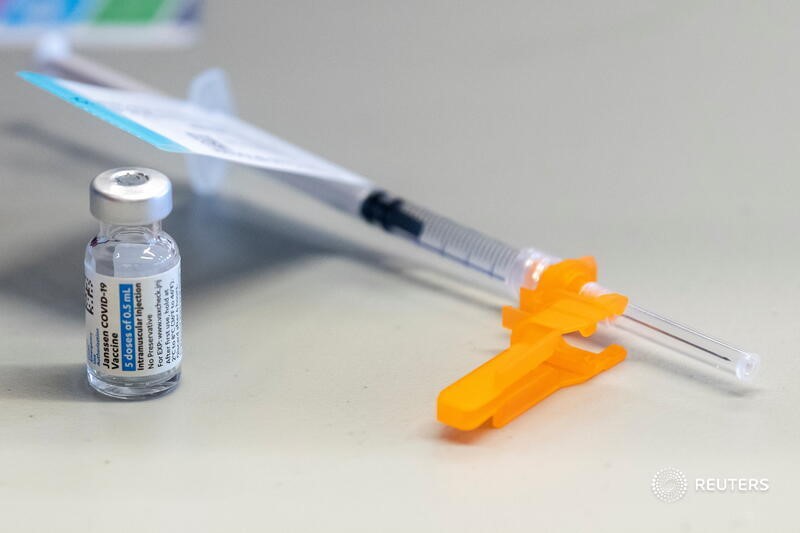
BRASÍLIA (Reuters) – Dirigentes da Agência Nacional de Vigilância Sanitária (Anvisa) reuniram-se na tarde desta sexta-feira com representantes da farmacêutica Janssen, da multinacional Johnson & Johnson, para discutir sobre a eventual extensão do prazo de validade da vacina contra a Covid-19 que será disponibilizada para o Brasil.
O Brasil deve receber nos próximos dias dos Estados Unidos um primeiro lote de 3 milhões de doses desse imunizante com data de validade de 27 de junho, disse o ministro da Saúde, Marcelo Queiroga, em recente depoimento à CPI da Covid do Senado.
+ Nos EUA, 60 milhões de doses da Janssen foram descartadas por contaminação
Segundo Queiroga, o lote da vacina da Janssen ainda precisa de autorização do FDA, espécie de Anvisa norte-americana, para ser enviado ao Brasil. Ele chegou a admitir a possibilidade de perda desses imunizantes, se houver demora no posicionamento do FDA.
Segundo a Anvisa afirma em comunicado nesta sexta, o prazo atual de validade da vacina avalizado pela agência é de três meses. A proposta da empresa é ampliar para quatro meses e meio. A FDA aprovou essa extensão na véspera.
Segundo o órgão regulador brasileiro, a equipe da Gerência-Geral de Medicamentos da Anvisa esclareceu dúvidas e se comprometeu a finalizar a análise das informações apresentadas pela Janssen o mais breve possível.
“Por se tratar de uma vacina com autorização para uso emergencial no Brasil, a decisão quanto ao pedido da farmacêutica caberá à Diretoria Colegiada da Anvisa, que deverá se reunir já na próxima semana”, informou a agência.
No final de março, a Anvisa autorizou o uso emergencial da vacina da Janssen no Brasil.
O país fechou um acordo no qual vai receber 38 milhões de doses desse imunizante, o único em uso no Brasil que será aplicado em dose única.
(Reportagem de Ricardo Brito)